G蛋白偶联受体(gpcr)在调节内环境的稳态中发挥关键作用,并作为细胞信号传导的主要介质与肿瘤进展密切相关。作为一个多样化和多功能的蛋白质群,G蛋白信号调节(RGS)家族被证明参与了gpcr的细胞转导。越来越多的证据表明,RGS蛋白失调是一种普遍现象,并强调了这些蛋白在人类癌症中的关键作用。此外,它们的差异表达可能是肿瘤诊断、治疗和预后的潜在生物标志物。最重要的是,目前关于RGS家族成员的功能/机制特征和临床应用的系统综述很少。在这篇综述中,我们重点介绍了g蛋白信号调节因子(RGS)家族,包括20多个家族成员。我们分析了RGS家族成员的分类、基本结构和主要功能。此外,我们还总结了RGS家族各成员在各种人类癌症中的表达变化及其在调节癌细胞增殖、干细胞维持、肿瘤发生和癌症转移中的重要作用。在此基础上,我们概述了一些RGS家族成员参与肿瘤进展的分子信号通路。最后讨论了它们在不同类型肿瘤的精确诊断、预后和治疗中的潜在应用,以及目前临床应用中可能存在的主要问题。我们的综述提供了对RGS在调节肿瘤进展中的作用和潜在机制的全面理解。
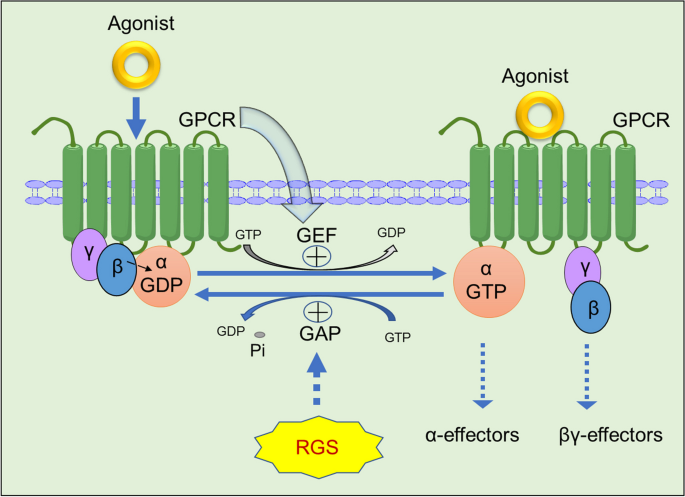
图书馆的src="http://www.hoppeake.com/news/ / / e.video-cdn.net/v2/embed.js " > 视频摘要 癌症是全世界人类死亡的主要原因之一。根据世界卫生组织下属的国际癌症研究机构(International Agency for Research on Cancer) 2021年发布的GLOBOCAN数据,2020年全球约有1930万新发癌症病例,约有1000万人死亡[1]。基因组结构和功能的累积改变驱动癌症的发展[2]。随着对肿瘤认识的不断深入,肿瘤的关键特征已被普遍化并不断更新[3]。与此同时,新的肿瘤相关标志物及其作用机制正在被发现。因此,有必要总结肿瘤相关蛋白介导癌症进展的典型机制和新发现的途径,以便实施更有针对性的干预措施,控制癌症进展,进一步降低癌症死亡率,延长患者生存期。 已有研究表明,G蛋白信号调节因子(RGS)蛋白可以作为GTP水解酶(gap)参与Gα- gdp和Gα-GTP异源三聚体(gpcr)的再循环过程。在没有激动剂的情况下,七跨膜G蛋白的α-亚基与GDP结合形成Gα-GDP, Gα-GDP与Gβγ异二聚体结合形成Gα-GDP/Gβγ闭环异三聚体。异源三聚体复合物进一步与G蛋白偶联受体(GPCR)相互作用。在这一过程中,GDP与Gα的结合减弱了GDP与GTP的自发交换活性。相反,Gβγ异源二聚体促进Gα与gpcr的偶联。在与激动剂结合后,gpcr发生构象变化,促进GTP在异三聚体的Gα亚基上的交换。活性形式的gtp结合的Gα和释放的Gβγ异二聚体随后都可以刺激相应的下游信号传导。当GAP存在时,它可以促进Gα-GTP中的小磷酸基水解,与GDP交换,重新形成Gα-GDP,然后恢复转变过程,形成Gα-GDP/Gβγ异源三聚体。RGS家族可以作为GAP,而不是调节GDP和GTP之间的酶促反应[4,5,6](图1)[7]。 图1 RGS蛋白对GPCR信号的典型调控模式。当G蛋白偶联受体(gpcr)特异性识别并结合激动剂时,gpcr引起构象变化,促进异源三聚体复合物α亚基上Gα- gdp的激活,以换取游离GTP,并释放Gβγ二聚体,这些二聚体都可以继续传导一些下游信号或效应器。RGS蛋白是Gα-GTP水解酶促进蛋白(gap),通过与GDP交换后促进Gα-GTP酶活性和GTP水解失活,促进异源三聚体复合物Gβγ与细胞膜上受体重组,从而终止gpcr的信号转导 近年来,GRCRs与多种疾病的发展有关。RGS蛋白作为GPCR信号传导的关键调控因子,在调节多种疾病的病理生理进程中也可能发挥重要作用。RGS超家族包含许多通过“RGS盒”结构域(也称为RH结构域)与Gα结合的调节因子,该结构域包含120个氨基酸特征[7]。在癌症进展过程中,这些RGS蛋白作为门控开关,对调节肿瘤细胞生长、增殖、分化和迁移至关重要[5,8,9]。然而,目前关于RGS家族成员在肿瘤中的功能/机制表征和临床应用的系统综述非常有限。 在本文中,我们综述了RGS家族各成员的最新报道,总结了RGS的历史和结构及其在癌症中的作用,并进一步讨论了控制RGS蛋白表达的分子机制,为未来新的靶向药物开发和相关癌症治疗提供见解。 哺乳动物G蛋白信号蛋白(RGS)包含20多个家族成员。基于序列同源性和不同的蛋白结构域,传统RGS家族可分为RGS A/RZ至RGS D/R12四个亚家族。每个亚家族包含多个成员,每个RGS蛋白包含大约120个氨基酸(RH)的一个或多个结构域,称为RGS盒,负责调节gtpase激活蛋白(GAP)的活性。反过来,GAP是GPCR周期中促进G蛋白失活的关键调控点。因此,RGS蛋白极大地增强了GAP的作用,使GTPase活性进一步提高了千倍(图2)[10]。 图2 经典RGS亚族及其相关结构域。基于RGS同源性和结构域,将经典RGS蛋白划分为4个亚家族。四个亚族分别是RGS A/RZ, B/R4, C/R7和D/R12,图中也列出了每个亚族的成员。除了RGS a /RZ亚家族中的半胱氨酸链(CYS)外,每个亚家族还包含一个G蛋白特异性RGS结构域(RH),即作用于Gα亚基并具有GAP活性的“RGS Box”。R4亚家族RGS3还存在PSD-95、Dlg和ZO-1/2 (PDZ)结构域;R7亚家族还包含disheveled /EGL10/pleckstrin结构域(DEP)和g蛋白γ样结构域(GGL);R12亚家族除含有PDZ结构域外,还含有磷酸酪氨酸结合域(PTB)、raf样ras结合域(RBD)和g蛋白调控基元(GoLoco) RGS A/RZ亚家族主要由RGS17、RGS19和RGS20三个成员组成,它们都是小而简单的蛋白,主要相关结构域半胱氨酸弦(cyys)位于n端附近,主要用于调节RGS蛋白的膜定位(图2和3A)。它主要用于调节膜定位,并作为结合位点与其他组分相互作用,分子量小,但保守稳定[11]。Garnier等人发现RGS17也被称为RGSZ2,几乎只在大脑中表达,在身体其他组织中很少表达[12]。但在癌症病理状态下,它在多种组织中均有显著表达。特别是通过高通量筛选等方法,许多研究发现RGS17是肺癌和前列腺癌的新靶点,其具体机制可能与RGS17通过调控cAMP-PKA-CREB通路诱导肿瘤细胞增殖有关[13,14,15,16]。也有报道称,RGS17在结直肠癌、肝细胞癌和宫颈癌组织及其细胞系中异常高表达[17,18,19],但有趣的是,RGS17在卵巢癌中显著降低,似乎具有肿瘤抑制基因的功能,这可能是由于RGS17的表达抑制了lpa介导的AKT激活途径[20](图4和5,表1)。 图3 RGS蛋白的基本结构和不同结构域。A RGS A/RZ亚族的基本结构域,包括RGS 17、RGS 19和RGS 20。红色:RGS- box (RGS域)。B RGS B/R4亚族的基本结构域,包括RGS 1-5、RGS 8、RGS13、RGS16、RGS18和rgs21。红色:RGS- box (RGS域)。RGS3:黄色表示C2域,红色表示RGS-Box域,紫色表示PDZ域。C RGS C/R7亚族的基本结构域,包括RGS6、RGS7、RGS9和RGS11。绿色:DEP结构域,灰色:G蛋白结构域,红色:RGS-Box。D RGS D/R12亚家族的基本结构域,包括RGS10、RGS12和RGS14。紫色:PDZ域,蓝色:PID域,红色:RGS-Box,绿色:RBD1域,黄色:RBD2域,橙色:Goloco域 图4 RGS家族蛋白在各种人类肿瘤类型中的表达综述。箭头表示各自肿瘤细胞的调控。主要关注的是本综述中描述的肿瘤(脑、肺、胃、肾细胞、结肠、卵巢、宫颈、甲状腺、乳腺、肝细胞、胰腺、膀胱、前列腺和黑色素瘤)中RGS的调节。这个图是经过许可创建的,由Figdraw绘制 图5 RGS家族成员作用的相关信号通路示意图 表1 RGS家族成员作为潜在的生物标志物及其在不同肿瘤类型中的作用 全尺寸工作台 RGS19比RGS17鲜为人知,这可能主要与其在机体正常稳态中的低表达水平有关。Michael E.等在前期研究中发现,RGS19可通过灭活Gα0来调节Wnt-β-catenin信号,而Gα0参与了生物体的许多生命过程[112],其中Wnt-β-catenin信号可促进小鼠心脏形成和心肌细胞分化。然而,在过表达RGS19的P19畸胎瘤细胞中,RGS19通过阻断Wnt信号传导抑制心肌细胞分化。Young Rae Ji等通过进一步研究RGS19过表达转基因小鼠(RGS19TG),证实RGS19影响心脏发育,负向调节心功能[113]。在人类实体瘤的发展过程中,RGS19似乎可以促进肿瘤细胞的原位增殖,同时抑制肿瘤细胞的迁移发育。根据癌症遗传图谱(TCGA)和DepMap数据库,RGS19已被报道在许多癌症中过表达,特别是在膀胱癌和卵巢癌中,RGS19可以通过增强AKT信号传导和免疫系统的细胞周期控制来实现无限制的细胞增殖。RGS19还调节cAMP/PKA/CREB通路,通过转录上调肿瘤转移抑制因子Nm23,从而减弱肿瘤细胞的迁移能力(图4和5,表1)。除此之外,可能还有更复杂的机制尚未报道,可能需要进一步探索和研究[24,25,114]。 RGS A/RZ亚家族,除了RGS17和RGS19外,也被称为RGSZ1或Ret RGS,选择性地与Gαi2和Gαz亚基结合并起作用。其表达与RGS19相似,在正常生物体中很少表达或不表达。然而,根据最近的报道,RGS20在各种癌症组织中的表达明显高于邻近的正常组织,如乳腺癌、转移性黑色素瘤、肝细胞癌和膀胱癌。李刚等通过MTT、不依赖锚定生长、荧光素酶活性等一系列生化实验及相关动物模型,发现RGS20可激活NF-κB信号。雷阳等通过在不同的人类癌细胞系中过表达和敲低RGS20,发现RGS20可以增加转移相关标志物的表达,下调粘附蛋白的表达,这可能表明RGS20的表达可以促进细胞增殖,增强癌细胞的侵袭性迁移能力[27,29,30](图4、5,表1)。 RGS1-5、RGS8、RGS13、RGS16、RGS18和RGS21是这四个亚家族中最丰富的成员。除分子量较大的RGS3外,其余成员的分子量均在20 ~ 30kd之间。RGS3分子量大的原因是其结构域由PDZ组成[115](图2和3B)。虽然R4家族成员的分子量普遍较小,但令人惊讶的是,这些蛋白质的主要结构域“RGS Box”能够识别并结合Gα的不同小亚基构象对其进行分类[116],这是R4成员参与GPCR循环的重要调节性点。由于RGS R4亚家族各成员的组织分布及其与生理和疾病的关系在之前的许多研究中都有报道[115,117],我们在这里主要总结其与每种实体瘤发展的关系。 RGS1是R4 RGS亚家族的重要成员,已被证明与多种b细胞活化和b细胞趋化因子调控诱导信号相关[118],主要参与免疫应答,干扰淋巴细胞的正常清除功能,造成免疫逃逸,为肿瘤细胞的发育提供有利的微环境[32]。然而,确切的机制尚不清楚。RGS1在多种实体肿瘤中显著上调,包括肾细胞瘤、黑色素瘤、卵巢癌和宫颈癌等[119]。研究表明,在黑色素瘤中,RGS1可以调节g αs介导的AKT和ERK磷酸化,促进黑色素瘤的发展;然而,有趣的是,这种调控并不参与gpcr中GTP的水解过程,它具有非gap功能[36,37]。此外,Javier Rangel等人也报道了RGS1表达上调与肿瘤厚度增加和有丝分裂率增加有关。虽然确切的作用机制仍有待发现,但可以肯定的是,RGS1促进肿瘤细胞的增殖、迁移和侵袭,并与弥漫性大b细胞淋巴瘤和多发性骨髓瘤的不良预后生存有关[38,120](图4和5,表1)。 与RGS1相比,RGS2表现出一些差异。在大多数实体肿瘤中,RGS2的表达普遍下调,这与RGS1的表达有很大的不同。RGS2特异性识别并倾向于结合Gαq亚基而不是其他家族成员来发挥GAP作用[45]。因此,RGS2比其他成员更具有抑制癌症发展的特性。乳腺癌组织中RGS2 mRNA的表达低于正常组,癌性乳腺细胞中RGS2的表达也低于正常乳腺细胞,其过表达可抑制乳腺癌细胞的生长,但其机制有待进一步探讨[39]。与邻近正常或增生组织相比,人前列腺癌标本中RGS2蛋白表达降低,RGS2可以调节erk1 /2介导的雄激素非依赖性雄激素受体(AR)的激活。X Cao等在此基础上提出RGS2可作为雄激素非依赖性前列腺癌细胞的生长抑制剂[46,121]。也有报道称RGS2表达可促进膀胱尿路上皮癌的迁移和侵袭能力,抑制膀胱尿路上皮癌中RGS2的表达为癌症的治疗提供了一个有希望的靶点[43]。而RGS2在其他肿瘤类型中的表达则相反,Yang S.等通过蛋白印迹和免疫荧光染色证实RGS2在胃癌细胞中的表达水平升高。胰腺癌分析也显示,RGS2与其他类型肿瘤的TMB、TID和CD8 + t细胞浸润有显著相关性[49](图4、5,表1)。 RGS3与R4家族其他成员的不同之处在于,除了“RGS Box”盒子外,其c端还存在PDZ结构域,使RGS3能够与GSK3β结合并抑制其活性,从而增强Wnt β-Catenin信号通路,从而促进上皮-间质转化(EMT)[122]。EMT与癌细胞的侵袭性和干细胞特性密切相关[123]。简而言之,RGS3增强了癌细胞的侵袭性和干细胞特性,并与非编码小rna相互作用,这对肿瘤细胞的发育很重要。例如,miR-25与RGS3表达呈负相关,其相互作用参与了非小细胞肺癌中癌细胞干细胞性的调控[58]。MiR-145-5p和RGS3在肝细胞癌中被正向促进,在促进细胞增殖和抑制细胞凋亡中发挥重要作用[60]。此外,microRNA-133a在胃癌中也与RGS3水平呈负相关,胃癌细胞和组织中RGS3的表达明显高于相应的正常组织和细胞[59](图4,表1)。 RGS4也是gpcr的负调控因子,它可以通过加速活性g - α- gtp的水解来阻断相关信号传导。RGS4可与不同的受体、效应器、支架蛋白等信号分子形成复杂的信号分子转导复合物,影响信号在细胞内的定位、活性和稳定性,在肿瘤组织或细胞中发挥重要的调节作用[61]。程传乐等研究发现RGS4在正常肺组织中的表达高于在非小细胞肺癌标本中的表达,相关分析表明RGS4的表达水平与淋巴结转移和TNM分期呈负相关,因此RGS4被认为是一种新的肿瘤抑制因子。在裸鼠转移模型中,RGS4过表达可抑制体内肿瘤的转移过程[62]。该蛋白在正常乳腺上皮细胞中也有显著表达,在乳腺癌细胞中沉默RGS4可增强癌细胞的侵袭能力。穆贤民等发现靶向药物在增加RGS4表达的同时,抑制了乳腺癌细胞中板样假足的形成、迁移和侵袭,其机制尚未阐明[61]。此外,RGS4在其他肿瘤类型中也表现出不具有上述功能的特征。例如,在骨肉瘤肿瘤组织中,RGS4与一种非编码RNA (miR-874-3p)相互作用,影响癌细胞的增值和迁移,RGS4过表达促进人骨肉瘤细胞的增值和迁移[124](图4和5,表1)。 RGS5是一种促进细胞凋亡和抵抗肿瘤细胞增殖的蛋白,也是RGS R4家族的成员,参与GPCR周期的负调控,是肿瘤相关周细胞的标志分子;然而,在肿瘤微环境中,促凋亡的RGS5可以受到其他调控信号的限制,甚至可以转化为抗凋亡的RGS5,从而提高周细胞的存活率,并且在几种癌症中的高表达与肿瘤生长和预后不良有关[125,126]。RGS5在大多数肝细胞癌组织样本和细胞系中高表达。Hu等研究表明,下调RGS5表达可显著抑制肝癌细胞的迁移和侵袭能力,而过表达可促进肝癌细胞上皮-间质转化的发生[127]。有证据表明RGS5可能参与调节GSK-3β活性和Wnt/β-catenin信号传导,影响肝细胞癌的发生发展[79]。此外,Dan Wang等研究表明,与正常卵巢组织相比,RGS5在上皮性卵巢癌中表达丰富,特别是在细胞质和微血管结构中表达(图4和5,表1)。然而,其潜在机制尚不清楚,可能与RGS5参与血管生成的调节有关[72]。 RGS16是R4家族的主要致癌基因之一,可促进多种人类肿瘤的恶性发展[87]。Ruoyu Huang等研究表明RGS16表达与胶质瘤分级呈正相关,RGS16过表达与胶质瘤细胞增殖、迁移、上皮-间质转化以及免疫和炎症反应密切相关[128]。此外,RGS16 mRNA和蛋白水平在结直肠癌组织中均高于正常组织;因此,RGS16可能被认为是结直肠癌和胰腺癌等癌症的预测标志物[88,90]。也有证据表明,抑制RGS16可直接或间接增强乳腺癌细胞的迁移和侵袭能力,但其潜在机制尚不清楚[87](图4和5,表1)。 RGS C/R7家族结构域不仅包含RGS Box (RH)结构域,还包含disheveled /EGL10/Pleckstrin结构域(DEP)和g蛋白γ样结构域(GGL)。DEP结构域结合R7结合蛋白(R7BP)等语法素样蛋白介导胞内定位,GGL结构域结合GB5亚基[5](图2和图3C)。R7亚家族包含4个主要成员:RGS6、RGS7、RGS9和RGS11。RGS6结构域负责RGS6和其他RGS蛋白的GAP活性,并允许其负向调节Gαi/o蛋白亚基,特异性参与多种癌症类型的发生和进展[95]。在结直肠癌和卵巢癌中,RGS6 mRNA和蛋白表达均降低,与肿瘤大小、CEA水平、TNM分期密切相关,更易发生淋巴结远处转移[99]。RGS6与细胞凋亡有关,介导细胞凋亡和化疗药物(阿霉素)等诱导的心肌病,与胰腺癌患者预后不良有关[129,130]。有趣的是,RGS6也被证明可以调节不依赖于G蛋白的信号传导。例如,在乳腺癌中,RGS6促进DNA甲基转移酶DNMT1的降解,从而阻止Ras系统发挥其促进细胞凋亡和抑制细胞增殖的重要功能[131,132](图4和5,表1)。 RGS7和RGS11也是R7家族的主要成员,它们可以参与gpcr的负调控,并与非典型G蛋白Gβ5形成一个成本稳定的复合物。RGS7和RGS11作为一种自我保护机制,可以抵抗化疗药物副作用引起的心肌纤维化,患者接受化疗后,心脏中RGS7和RGS11的表达增加,但其机制尚不清楚[133,134]。RGS7最初定位为肿瘤抑制因子,在黑色素瘤中不稳定,容易发生反复突变,从而促进黑色素瘤细胞的迁移和侵袭,这可能与RGS7催化Gα-GTP水解活性降低以及蛋白本身的不稳定性有关[101]。杨盛辉等发现RGS11在肺腺癌患者的淋巴结和骨转移灶中高表达,但有趣的是,RGS11表达的增强和减弱揭示了其仅在细胞迁移中起特定作用,与细胞侵袭或增殖没有相关报道[101]。胡岳欣等利用KM-plotter数据库发现RGS11在卵巢癌中过表达,促进卵巢癌的发生进展,但具体机制尚未探讨[34](图4、5,表1)。 与其他三个亚家族不同,RGS D/R12亚家族包含的家族成员差异很大,其中RGS10是一个相对简单的RGS蛋白,大小为20 kDa,而RGS12和RGS14比RGS10大得多,也复杂得多。RGS12和RGS14具有串联ras结合域(RBD)和c端GoLoco基序(GoLoco),它们是Gai/o亚基的鸟嘌呤核苷酸解离抑制剂(gdi)[5](图2和3D)。Feyzanur Yildirimtepe等人发现RGS10在正常结直肠组织中的表达高于肿瘤组织,DNA甲基化与RGS10转录物呈负相关[104]。在卵巢癌细胞中,抑制RGS10的表达可促进AKT信号通路的激活,导致细胞增殖增强,进而促进卵巢癌的进展。因此,RGS10可能是治疗癌症的关键靶点之一[105](图4,表1)。 RGS12具有额外的n端基序,包括PSD-95/DLG/ZO1 (PDZ)结构域和磷酸酪氨酸结合(PTB)结构域,是分子量最高的经典RGS蛋白家族成员(图3D)。PSD-95/DLG/ZO1 (PDZ)结构域可与丝裂原活化蛋白激酶(MEK2)结合,PTB结构域(PTB)可与n型钙通道结合。RGS12参与调节体内多种重要的传递,这对正常组织和肿瘤细胞都很重要[128]。王永泉等人在非洲裔美国人的前列腺癌组织和细胞中发现RGS12蛋白低表达,并证明RGS12作为一种新型肿瘤抑制因子可以抑制AKT和MNX1信号通路[109]。RGS12还可通过抑制骨肉瘤其他相关标志物的表达和功能,在骨肉瘤中发挥抑瘤作用[111]。C Fu等研究表明,在口腔鳞状细胞癌中敲低RGS12可显著增加转基因小鼠的癌细胞增殖和迁移,RGS12可使AKT/mTOR信号通路失活,从而抑制肿瘤细胞的发育[110](图4和5,表1)。综上所述,这些发现表明RGS12可作为肿瘤抑制因子,是治疗各种癌症的一个新的有希望的靶点。 R4亚家族的RGS8、RGS18和RGS21, R7亚家族的RGS9和R12亚家族的RGS14对肿瘤和癌症的生物学影响尚未有系统的报道。R4亚家族的RGS13仅作为B淋巴瘤中尖锐湿疣淋巴瘤(condyloma lymphoma, MCL)的新的特异性标记物,RGS13在MCL中的作用机制尚未阐明[85]。然而,其对肿瘤/癌细胞产生和发展的潜在影响以及靶向癌症治疗的高价值将在未来进一步探索。 摘要。 背景 有限公司 结论和观点 数据和材料的可用性 参考文献。 致谢。 作者信息 道德声明 # # # # # RGS蛋白在癌症进展中起着至关重要的作用,其在癌症中的作用与蛋白质结构密切相关。所有四个RGS亚群都包含RGS盒(RH)特征基序,并参与多种癌症中的增殖、凋亡、迁移和激酶信号传导,这表明该基序可能有助于它们在肿瘤激酶信号传导中的作用。这四个亚群之间存在一些结构上的差异,因此,它们也有一些功能上的差异。即使是同一亚群的成员也表现出一些功能上的差异;例如,B/R4亚群中的RGS2和RGS4在多种肿瘤中低表达[41,49,62,63],而RGS1和RGS5在大多数肿瘤类型中高表达[32,35,72,73](表1)。这可能是由于其他结构差异导致的功能变化,这需要进一步研究。 目前对肿瘤中RGS蛋白的研究主要集中在表型因素上,如RGS在细胞增殖、凋亡、坏死、转移和耐药中的抑制或促进作用[15,17,76,81]。令人困惑的是,尽管RGS蛋白具有相似的保守结构域,但一些RGS蛋白具有促癌特性,而另一些RGS蛋白具有相反的作用。例如,一些RGS蛋白,即RGS1、RGS3、RGS5和RGS13具有促肿瘤作用,而另一些蛋白,即RGS2、RGS4、RGS6、RGS10和RGS12具有抑制肿瘤作用。这可能是由于不同肿瘤中未被发现的结构差异或特定结构变化。此外,根据肿瘤类型的不同,一些RGS蛋白同时具有抑制肿瘤和促进肿瘤的作用,这可能是其在不同肿瘤类型中作用不同的机制。例如,RGS16在结直肠癌中具有促肿瘤作用,是潜在的诊断标志物[88],而在乳腺癌中则通过抑制PI3K信号通路起到抑制肿瘤的作用[87]。在介导GPCR信号传导过程中,RGS蛋白可能影响多种激酶的激活或失活。然而,到目前为止,直接受RGS蛋白影响的激酶仍然未知,RGS蛋白在癌症进展中的具体分子机制尚未全面确定。因此,需要更深入的研究来阐明RGS蛋白的确切功能,探索其在癌症中的分子机制,为更有效的癌症治疗提供理论依据。此外,大多数RGS蛋白已被报道与患者预后相关,这表明RGS蛋白是癌症治疗的潜在生物标志物。 众所周知,开发治疗癌症的有效药物是至关重要的。目前,根据以往的报道,RGS蛋白在癌症中的功能作用在不同的肿瘤类型之间似乎也没有显著的特异性。为了进一步确定RGS在不同人类癌症中的四个亚组的特异性,研究人员利用在线数据库结合研究报告分析了RGS在各种癌症中的表达。研究发现,不同的RGS亚群对某些癌症具有显著的特异性(表1,图4),这可能有助于其诊断和治疗。此外,由于RGS蛋白的结构多样性,很难产生单一RGS蛋白的抑制剂。因此,迫切需要进一步寻找新的方法来生产针对RGS蛋白的有效药物,从而为癌症治疗做出贡献,并影响其他领域的药物开发。 ccDownload: /内容/ pdf / 10.1186 / s12964 - 023 - 01334 - 7. - pdf